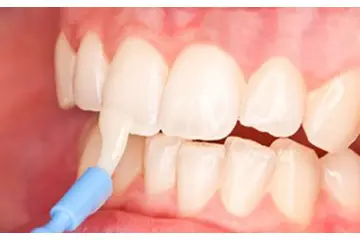
Baş Kuantum Sayısı Kaçtır?
Bu içerik, baş kuantum sayısının atomik yapıdaki rolünü ve önemini ele almaktadır. Elektronların enerji seviyelerini belirleyen bu temel parametre, atomların kimyasal özellikleri ve reaktivitesi üzerinde etkili olur. Kuantum mekaniği açısından, baş kuantum sayısının anlaşılması, modern fizik ve kimya alanındaki gelişmeler için gereklidir.
Baş Kuantum Sayısı Nedir?Baş kuantum sayısı, atomik yapının önemli bir parçası olan kuantum mekaniği çerçevesinde, bir elektronun bir atom içerisindeki enerji seviyelerini belirleyen temel bir parametredir. Baş kuantum sayısı, genellikle "n" harfi ile gösterilir ve pozitif tam sayılar olarak 1, 2, 3,... şeklinde tanımlanır. Bu sayı, elektronun bulunduğu atom orbitallerinin büyüklüğünü ve enerji seviyesini belirler. Baş Kuantum Sayısının Fiziksel Anlamı Baş kuantum sayısının fiziksel anlamı, elektronun atom çekirdeğinden ne kadar uzakta olduğunu gösterir. Daha yüksek bir baş kuantum sayısı, elektronun daha yüksek bir enerji seviyesinde bulunduğunu ve atom çekirdeğinden daha uzak bir konumda olduğunu ifade eder. Bu durum, atomun kimyasal özellikleri üzerinde de etkili olur. Baş Kuantum Sayısının Değerleri ve Anlamları Baş kuantum sayısının değerleri aşağıdaki gibidir:
Baş Kuantum Sayısı ve Diğer Kuantum Sayıları Baş kuantum sayısı, atomdaki elektronların konumunu belirlemek için kullanılan diğer kuantum sayılarıyla birlikte çalışır. Bunlar arasında:
Bu kuantum sayıları birlikte, bir elektronun durumunu tam olarak tanımlamak için gereklidir. Atomik Yapı Üzerindeki Etkileri Baş kuantum sayısı, atomların kimyasal özellikleri ve reaktivitesi üzerinde belirleyici bir etkiye sahiptir. Örneğin, baş kuantum sayısının yüksekliği, atomun daha fazla enerji seviyesine sahip olmasına ve dolayısıyla daha karmaşık kimyasal bağlar kurabilmesine olanak tanır. Sonuç Baş kuantum sayısı, atomik yapının ve elektronların davranışının anlaşılmasında hayati bir rol oynamaktadır. Kuantum mekaniğinin temellerini anlamak, atomların fiziksel ve kimyasal özelliklerini açıklamak için gereklidir. Bu sayede, modern kimya ve fizik alanlarındaki birçok gelişme ve uygulama mümkün hale gelmiştir. Ekstra Bilgiler Baş kuantum sayısı, atomlar arası etkileşimleri ve moleküllerin yapısını anlamada da önemli bir yere sahiptir. Ayrıca, baş kuantum sayısının etkileri, yüksek enerjili fizik deneylerinde ve kuantum bilgisayarlarındaki uygulamalarda da gözlemlenmektedir. Bu nedenle, baş kuantum sayısı, sadece temel bilimler açısından değil, aynı zamanda uygulamalı bilimler ve teknoloji açısından da büyük bir öneme sahiptir. |
.webp)








.webp)
.webp)









.webp)


.webp)
.webp)

.webp)










Baš kuantum sayısının yalnızca pozitif tam sayılar almasının altında yatan mantığı anlamak oldukça ilginç. Bu sayının, atomun enerji seviyelerini belirlemesi ve elektronların çekirdekten ortalama uzaklıklarını tayin etmesi, atom modelinin temel taşlarından birini oluşturuyor. Pozitif tam sayılar kullanılarak belirlenen bu seviyeler, atomun kararlılığını ve kimyasal davranışını doğrudan etkiliyor. Özellikle, baş kuantum sayısı arttıkça elektronların enerji seviyeleri de artıyor ve bu durum, elektronların çekirdekten daha uzak bölgelerde bulunmalarını sağlıyor. Daha yüksek enerji seviyelerinde bulunan elektronlar, kimyasal reaksiyonlarda daha aktif hale gelebiliyorlar. Bu da atomların nasıl etkileşime girdiğini ve reaksiyonların nasıl gerçekleştiğini anlamak için kritik bir öneme sahip. Aynı zamanda, bu durumun kimyasal bağlar üzerindeki etkisini de sorgulamak gerekiyor. Elektronların daha yüksek enerji seviyelerine çıkması, atomların birbirleriyle etkileşimlerini ve bağ kurma yeteneklerini değiştirebilir. Bu nedenle, baş kuantum sayısının değerleri, özellikle karmaşık moleküllerin ve bileşiklerin davranışlarını anlamada kilit bir rol oynuyor. Bu karmaşık ilişkiler, kimyasal tepkimelerin dinamiklerini ve atomların nasıl bir araya geldiğini çözmek için önemli bir temel sağlıyor.
Baş Kuantum Sayısı ve Atomun Enerji Seviyeleri
Süsen, baş kuantum sayısının yalnızca pozitif tam sayılar almasının arkasındaki mantık gerçekten de ilginçtir. Bu sayının atomun enerji seviyelerini belirlemesi ve elektronların çekirdekten ortalama uzaklıklarını tayin etmesi, atom modelinin temel taşlarından biridir. Pozitif tam sayılarla belirlenen bu seviyeler, atomun kararlılığını ve kimyasal davranışını doğrudan etkileyerek önemli bir rol oynar.
Enerji Seviyelerinin Artışı
Baş kuantum sayısı arttıkça, elektronların enerji seviyeleri de artar. Bu durum, elektronların çekirdekten daha uzak bölgelerde bulunmalarını sağlar. Daha yüksek enerji seviyelerinde bulunan elektronlar, kimyasal reaksiyonlarda daha aktif hale gelebilirler. Bu da atomların nasıl etkileşime girdiğini ve reaksiyonların nasıl gerçekleştiğini anlamak açısından kritik bir öneme sahiptir.
Kimyasal Bağlar Üzerindeki Etkileri
Aynı zamanda, baş kuantum sayısının değerlerinin kimyasal bağlar üzerindeki etkisini sorgulamak da gereklidir. Elektronların daha yüksek enerji seviyelerine çıkması, atomların birbirleriyle etkileşimlerini ve bağ kurma yeteneklerini değiştirebilir. Bu nedenle, baş kuantum sayısının değerleri, özellikle karmaşık moleküllerin ve bileşiklerin davranışlarını anlamada kilit bir rol oynamaktadır. Bu karmaşık ilişkiler, kimyasal tepkimelerin dinamiklerini ve atomların nasıl bir araya geldiğini çözmek için önemli bir temel sunmaktadır.
Baş kuantum sayısının enerji seviyelerini belirlerken neden sadece pozitif tam sayılar aldığını açık bir şekilde anlayamıyorum. Bu enerji seviyelerinin atomun genel davranışına etkisi ne kadar büyük? Herhangi bir elektronun, baş kuantum sayısı artıkça çekirdekten uzaklaştığında neden daha fazla enerjiye sahip olduğunu merak ediyorum. Bu durumun kimyasal reaksiyonlar üzerindeki etkileri nasıl oluyor?
İçkin,
Baş kuantum sayısının sadece pozitif tam sayılar alıyor olması, atomik orbitallerin matematiksel tanımı ve Schrödinger denkleminin çözümlerine dayanır. Bu çözümler, elektronların belirli enerji seviyelerinde bulunabileceklerini gösterir ve bu seviyeler pozitif tam sayılarla ifade edilir. Negatif veya sıfır değerler, fiziksel olarak anlamlı olmayan durumları temsil eder.
Enerji Seviyeleri ve Atomun Davranışı: Baş kuantum sayısı, elektronun enerji seviyesini belirler ve bu enerji seviyeleri atomun kimyasal ve fiziksel özelliklerine doğrudan etki eder. Yüksek baş kuantum sayısına sahip elektronlar, çekirdekten daha uzak olurlar ve bu nedenle daha yüksek enerjiye sahip olurlar. Bu, elektronların çekirdek tarafından daha az güçlü bir şekilde çekilmesiyle ilgilidir.
Kimyasal Reaksiyonlara Etkisi: Elektronların enerji seviyeleri, atomların kimyasal reaksiyonlarda nasıl etkileşime gireceğini belirler. Dış katmandaki (valans) elektronları, atomların diğer atomlarla bağ yapma yeteneğini etkiler. Yüksek enerji seviyesindeki elektronlar, daha kolay iş birliğine girerler ve kimyasal reaksiyonlarda daha aktif rol oynarlar.
Umarım bu açıklamalar kafanÄdaki sorularınÄ yanıtlamıştır.
Sevgiler,
[Adın]