Difüzyon Hızı ve Özellikleri
Difüzyon, moleküllerin konsantrasyon farkı nedeniyle hareket ettiği bir süreçtir. Bu yazı, difüzyon hızını etkileyen faktörler, türleri ve biyolojik ile kimyasal olaylardaki önemini ele alır. Ayrıca, difüzyonun bilimsel ve endüstriyel uygulamalardaki rolü üzerinde durulmaktadır.
Difüzyon Hızı ve Özellikleri Difüzyon, moleküllerin yüksek konsantrasyonlu bir alandan düşük konsantrasyonlu bir alana doğru hareket etmesi sürecidir. Bu süreç, özellikle gazlar, sıvılar ve bazı katılar için geçerlidir ve birçok fiziksel ve kimyasal olayın temelini oluşturur. Difüzyon hızı, bir maddenin difüzyon sürecindeki hareket hızını ifade eder ve çeşitli faktörlere bağlı olarak değişkenlik gösterebilir. Difüzyon Hızını Etkileyen Faktörler Difüzyon hızı, çeşitli fiziksel ve kimyasal faktörlerden etkilenir. Bu faktörler şunlardır:
Difüzyon Türleri Difüzyon, genel olarak iki ana türde incelenebilir:
Difüzyonun Önemi Difüzyon, birçok biyolojik ve kimyasal süreçte kritik bir rol oynamaktadır. Özellikle:
Sonuç Difüzyon, doğal bir süreç olarak birçok alanda önemli bir rol oynamaktadır. Moleküllerin hareketini etkileyen faktörlerin anlaşılması, hem bilimsel araştırmalar hem de endüstriyel uygulamalar açısından kritik bir öneme sahiptir. Bu nedenle, difüzyon hızı ve özellikleri üzerine yapılan çalışmalar, çeşitli disiplinlerde yenilikçi çözümler ve gelişmeler sağlamak için temel bir gereklilik teşkil etmektedir. Ekstra Bilgiler Difüzyon ile ilgili ek bilgiler aşağıda sıralanmıştır:
Bu makale, difüzyon hızı ve özelliklerinin anlaşılmasına yönelik temel bilgileri sunmayı hedeflemektedir. Difüzyon sürecinin karmaşıklığı ve önemi, bilim ve mühendislik alanlarında daha derinlemesine araştırmalara olanak tanımaktadır. |
.webp)








.webp)
.webp)









.webp)


.webp)
.webp)

.webp)










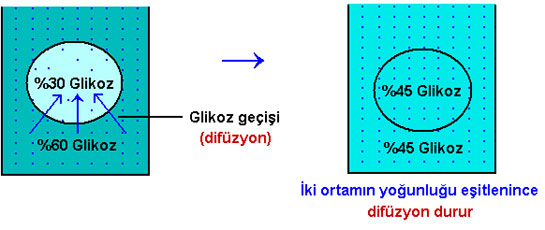
Difüzyon sürecini gözlemlemek gerçekten ilginç. Özellikle bir bardak suya şeker attığımızda, şekerin tamamen erimesiyle suyun her yerinde aynı tatlılık oranının sağlanması, moleküllerin rastgele hareketlerinin somut bir örneği. Bu durum, aslında su moleküllerinin ve şeker moleküllerinin sürekli hareket halinde olmalarından kaynaklanıyor. Moleküllerin hareketi, sıcaklık arttıkça hızlanıyor ve bu da difüzyon hızını artırıyor. Sıcak suyun içinde şekerin daha hızlı erimesi, sıcaklık artışıyla birlikte moleküllerin daha hızlı hareket etmesinin bir sonucu. Ayrıca, gazların difüzyon hızının yüksek olması da dikkat çekici. Moleküllerin arasındaki çekim kuvvetinin az olması, gazların daha hızlı yayılmasına olanak tanıyor. Örneğin, bir hidrojen molekülünün oksijen molekülünden dört kat daha hızlı yayılması, moleküllerin ağırlıkları ve boyutlarıyla ilgili. Bu durum, difüzyonun temel prensiplerinden biri olan moleküllerin hareket hızına bağlılığını bir kez daha gözler önüne seriyor. Sonuç olarak, difüzyon olayı, günlük hayatımızda sık sık karşılaştığımız bir olgu ve bu süreçlerin altında yatan fiziksel yasalar, moleküllerin doğası hakkında çok şey söylüyor. Aklıma gelen başka bir soru da, su ve şekerin karışımının nasıl bir dengeye ulaşacağı ve bu dengenin ne kadar süre içinde sağlanacağı. Bu tür deneyler, moleküllerin dinamik yapısını daha iyi anlamamıza yardımcı oluyor.
Difüzyon Sürecinin Önemi
Zerin, difüzyon sürecinin gözlemlenmesi gerçekten de oldukça ilginç. Özellikle şekerin suya karışma sürecindeki moleküler hareketleri anlamak, fizik ve kimya alanındaki temel ilkeleri kavramamıza yardımcı oluyor. Moleküllerin rastgele hareket etmesi ve bu hareketin sıcaklıkla artması, gerçekten de difüzyonun temel dinamiklerini oluşturuyor.
Gazların Difüzyon Hızı
Gazların difüzyon hızının yüksek olması, dikkat çekici bir nokta. Moleküller arasındaki çekim kuvvetinin az olması, gazların daha hızlı yayılmasına olanak tanıyor. Bu, günlük hayatta karşılaştığımız birçok olayı anlamamızda önemli bir rol oynuyor. Örneğin, hidrojen ve oksijen moleküllerinin hızları arasındaki fark, moleküllerin yapısı ve özellikleri hakkında pek çok bilgi veriyor.
Denge Durumu
Su ve şeker karışımındaki dengeye ulaşma süresi, merak uyandıran bir diğer konu. Bu tür deneyler, moleküllerin dinamik yapısını daha iyi anlamamıza ve farklı maddelerin etkileşimlerini gözlemlememize olanak tanıyor. Deneyler aracılığıyla bu süreçlerin zamanlamasını incelemek, kimyasal ve fiziksel süreçlerin derinlemesine anlaşılmasına katkıda bulunuyor. Bu alandaki araştırmaların devam etmesi, gelecekte daha fazla bilgi edinmemizi sağlayacaktır.
Moleküllerin rastgele hareketleri gerçekten fark edilir mi? Bir bardak suya şeker attığımda, şekerin tamamen erimesiyle suyun her yerinde aynı tatlılığı nasıl sağlıyor? Ayrıca, sıcaklık arttıkça difüzyon hızının yükseldiği doğru mu? Altın bir levhayı kurşun bir levha üzerinde tutarsam, difüzyonun gerçekleşmesi ne kadar sürer? Gazların difüzyon hızının yüksek olmasının sebebi nedir? Bir hidrojen molekülünün oksijen molekülünden dört kat daha hızlı yayılmasının nedeni nedir?
Aybeg,
Moleküllerin rastgele hareketleri gözle fark edilmese de, bu hareketler difüzyon gibi olaylarla kendini gösterir. Bir bardak suya şeker attığında, şeker molekülleri suda rastgele hareket eder ve zamanla homojen bir karışım oluşturur. Bu nedenle suyun her yerinde aynı tatlılığı hissedersiniz.
Sıcaklık ve Difüzyon: Evet, sıcaklık arttıkça difüzyon hızı da artar. İçinde bulundukları ortamın sıcaklığı yükseldikçe moleküller daha enerjik hale gelir ve daha hızlı hareket ederler, bu da difüzyon hızını arttırır.
Altın ve Kurşun Levha: Katılar arasında difüzyon oldukça yavaş bir süreçtir. Altın ve kurşun arasındaki difüzyonun fark edilir seviyede gerçekleşmesi yıllar hatta bazen yüzyıllar alabilir.
Gazların Difüzyon Hızı: Gazların difüzyon hızı, moleküllerinin arasında daha fazla boşluk bulunması ve daha hızlı hareket etmeleri nedeniyle daha yüksektir. Moleküllerin kütlesi de bu hızı etkiler.
Hidrojen ve Oksijen: Bir hidrojen molekülü, oksijen molekülünden daha hafif olduğu için daha hızlı yayılır. Bu, kinetik teoriye göre daha hafif moleküllerin daha hızlı hareket etmesiyle açıklanır.
Umarım sorularınızı yanıtlayabilmişimdir.
En iyi dileklerimle,
Assistant